

新疆农业科学 ›› 2023, Vol. 60 ›› Issue (6): 1460-1465.DOI: 10.6048/j.issn.1001-4330.2023.06.019
刘江娜( ), 张西英, 李荣霞, 张小伟, 白云凤, 张爱萍(
), 张西英, 李荣霞, 张小伟, 白云凤, 张爱萍( )
)
收稿日期:2022-10-07
出版日期:2023-06-20
发布日期:2023-06-20
通信作者:
张爱萍(1968-),女,安徽人,研究员,研究方向为植物分子育种,(E-mail) 592354963@qq.com
作者简介:刘江娜(1985-),女,河北人,硕士,副研究员,研究方向为植物分子育种,(E-mail)2849847373@qq.com
基金资助:
LIU Jiangna( ), ZHANG Xiying, LI Rongxia, ZHANG Xiaowei, BAI Yunfeng, ZHANG Aiping(
), ZHANG Xiying, LI Rongxia, ZHANG Xiaowei, BAI Yunfeng, ZHANG Aiping( )
)
Received:2022-10-07
Online:2023-06-20
Published:2023-06-20
Correspondence author:
ZHANG Aiping(1968-), female, bachelor, researcher, mainly engaged in plant molecular breeding, (E-mail) 592354963@qq.com
Supported by:摘要:
【目的】番茄红素合成后会在β-番茄红素环化酶SlLCY-B(lycopene-β-cyclase)催化下进入代谢途径,抑制SlLCY-B2的表达可增加番茄红素的积累。对番茄红素代谢调控基因SlLCY-B1的分子特征及sgRNA进行系统分析,为利用CRISPR/ Cas9 技术对SlLCY-B2及其上游启动子序列进行定点突变或片段删除、调控SlLCY-B2的表达以减少代谢的途径,提高番茄果实的番茄红素含量。【方法】利用生物在线工具,对SlLCY-B2多肽特性及保守结构域、基因组结构、数字表达谱、启动子顺式作用元件进行系统分析,根据CRISPR-Cas9靶点设计原则,设计筛选出适宜的sgRNA。【结果】SlLCY-B2位于番茄6号染色体,编码498 个氨基酸,gDNA不含内含子,呈果实特异性表达。SlLCY-B2分布145条sgRNA,其中21条有高特异性。SlLCY-B2上游-1 500 bp 启动子序列分布15个顺式作用元件和112条sgRNA。【结论】对SlLCY-B2和其启动子区进行基因编辑,可调控SlLCY-B2的表达,将提高番茄红素含量。
中图分类号:
刘江娜, 张西英, 李荣霞, 张小伟, 白云凤, 张爱萍. 番茄SlLCY-B2及其启动子的分子特征和sgRNA分析[J]. 新疆农业科学, 2023, 60(6): 1460-1465.
LIU Jiangna, ZHANG Xiying, LI Rongxia, ZHANG Xiaowei, BAI Yunfeng, ZHANG Aiping. Molecular characteristics and promoter analysis of SlLCY-B2 gene in tomato[J]. Xinjiang Agricultural Sciences, 2023, 60(6): 1460-1465.
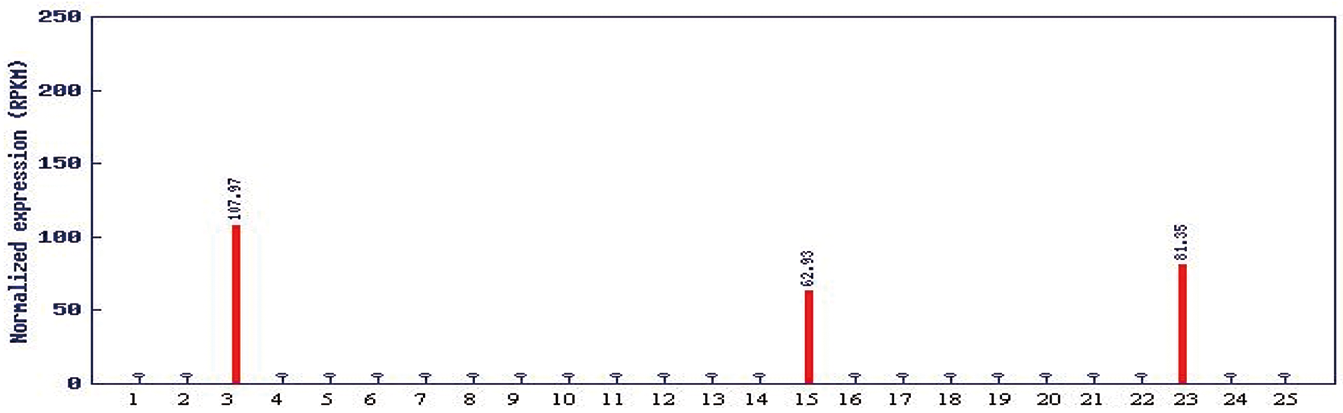
图1 基于 RNA-seq的SlLCY-B2数字表达谱 注:1.果实,子房; 2.未成熟绿果; 3.成熟绿果; 4.破色期果实; 5.成熟红果; 6.花蕾(0~3 mm); 7.花蕾(3~8 mm); 8.开花前花蕾(8 mm); 9.开放的花; 10.发育阶段花的混合物; 11.野生番茄花粉; 12.感染假单胞菌叶片;13.抗假单胞菌叶片;14.混合诱导叶片;15.植株的顶端分生组织(4~6周龄植株); 16.植株顶端分生组织(8周龄植株);17.花前根;18.挂果期根;19.营养匮乏的根;20.完全吸涨5 d后的胚根;21.完全吸涨7 d后的幼苗;22.休眠种子; 23.愈伤组织;24.悬浮培养物;25.冠瘿。PRKM: 每百万reads中来自于特定基因每千碱基长度的reads数
Fig.1 The digital expression profile of SlLCY-B2 baded on RNA-sequence Note: 1.TA496 fruit, ovary; 2.TA496 fruit,developing/immature green; 3.TA496 fruit, mature green; 4.TA496 fruit, breaker 5.TA496 fruit, red ripe; 6.TA496 flower, 0-3 mm buds; 7.TA496 flower, 3-8 mm buds; 8.TA496 flower, 8 mm-preanthesis buds; 9.TA496 open flower; 10.TA496 flower, a mixture of developmental stages (mixed flower); 11.TA56 wild tomato pollen; 12.R11-13 (Rio Grande x Money Maker) leaf, Pseudomonas susceptible; 13.R11-12 (35S::Pto in Rio Grande x Money Maker) leaf, Pseudomonas resistant; 14.Rio Grande PtoR leaf, mixed elicitor; 15. TA496 shoot/meristem, 4-6 week old plants; 16.TA496 shoot meristem, 8 week old plants; 17.TA496 root, plant at pre-anthesis; 18.TA496 root, plant at fruit set; 19.TA496 root, nutrient deficient; 20.TA496 radicle, seedlings 5 days post-imbibition; 21.TA496 whole seedling,7 days post imbibtion; 22.TA496 quiescent seed; 23.TA496 callus; 24.TA496, E6203 Suspension culture; 25.TA496 crown gall. PRKM: Reads Per Kilo bases per Million reads
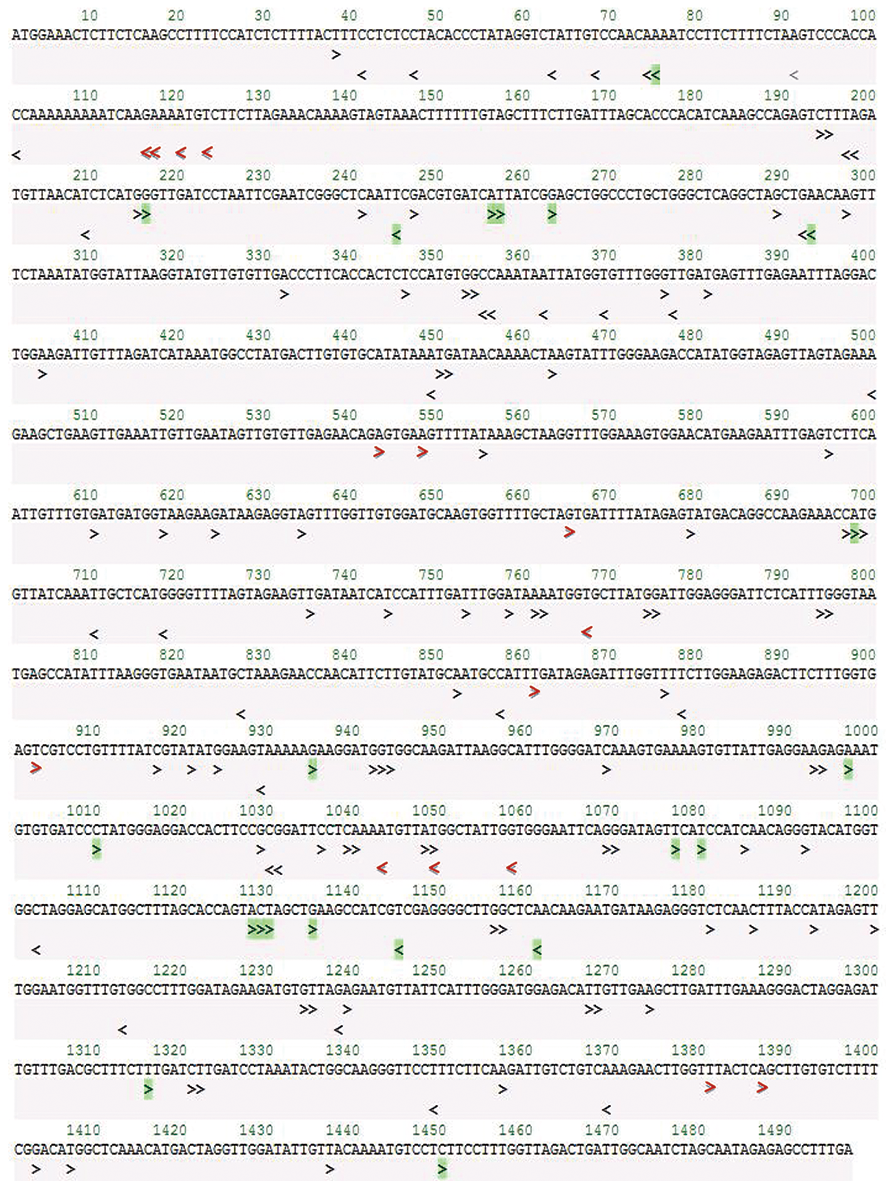
图3 sgRNA在SlLCY-B2的分布 注:绿色>示这些sgRNAs位于外显子绿色示sgRNA邻近PAM 12 nt的种子序列在番茄全基因组上是唯一序列;黑色>色示该sgRNA邻近PAM 12 nt 的种子序列在其它染色体的1个位点上有与其匹配的序列;红色<表示这些sgRNAs横跨2个外显子邻接处或含有含连续的TTTT,选用pol III启动子尽力避免选用这些sgRNA序列
Fig.3 The position of sgRNAs in SlLCY-B2 Note:Green shows these sgRNAs located in exon green seed sequence on the whole tomato genome; blue shows the seed sequence of the sgRNA adjacent PAM 12 nt has a matching sequence at one site of other chromosomes; grey indicates these sgRNAs across two exon neighbors or containing continuous TTTT, using pol III promoter to avoid these sgRNA sequences
| 元件 Elements | 序列及位置 Sequences and position | 数量 Number | 功能 Function |
|---|---|---|---|
| A-box | CCGTCC: -598 | 1 | 顺式调控元件 |
| GATA-motif | AAGGATAAGG: -1048 | 1 | 部分光响应元件 |
| GT1-motif | GGTTAAT: - 27, | 1 | 光响应元件 |
| GT1-motif | GGTTAA: - 27, | 1 | 光响应元件 |
| I-box | atGATAAGGTC: -1046 | 1 | 部分光响应元件 |
| LTR | CCGAAA : -378,-707 | 2 | 低温响应顺式调控元件 |
| MBS | CAACTG:- 439 | 1 | 与干旱诱导相关的 MYB 结合位点 |
| P-box | CCTTTTG:-914,-1346 | 2 | 赤霉素响应元件 |
| P-box | CAACAAACCCCTT: -1290 | 1 | 赤霉素响应元件和部分光响应元件 |
| TC-rich repeats | ATTCTCTAAC: -1402 | 1 | 防御和胁迫响应顺式调控元件 |
| TGA-element | AACGAC:-990 | 1 | 生长素响应元件 |
| chs-CMA2a | TCACTTGA: -759 | 1 | 部分光响应元件 |
| Circadian | CAAAGATATC: -289 | 1 | 昼夜节律控制顺式调控元件 |
表1 SlLCY-B2启动子顺式作用元件
Tab.1 Predicted cis-regulatory elements in SlLCY-B2 promoter
| 元件 Elements | 序列及位置 Sequences and position | 数量 Number | 功能 Function |
|---|---|---|---|
| A-box | CCGTCC: -598 | 1 | 顺式调控元件 |
| GATA-motif | AAGGATAAGG: -1048 | 1 | 部分光响应元件 |
| GT1-motif | GGTTAAT: - 27, | 1 | 光响应元件 |
| GT1-motif | GGTTAA: - 27, | 1 | 光响应元件 |
| I-box | atGATAAGGTC: -1046 | 1 | 部分光响应元件 |
| LTR | CCGAAA : -378,-707 | 2 | 低温响应顺式调控元件 |
| MBS | CAACTG:- 439 | 1 | 与干旱诱导相关的 MYB 结合位点 |
| P-box | CCTTTTG:-914,-1346 | 2 | 赤霉素响应元件 |
| P-box | CAACAAACCCCTT: -1290 | 1 | 赤霉素响应元件和部分光响应元件 |
| TC-rich repeats | ATTCTCTAAC: -1402 | 1 | 防御和胁迫响应顺式调控元件 |
| TGA-element | AACGAC:-990 | 1 | 生长素响应元件 |
| chs-CMA2a | TCACTTGA: -759 | 1 | 部分光响应元件 |
| Circadian | CAAAGATATC: -289 | 1 | 昼夜节律控制顺式调控元件 |

图4 sgRNA和顺式作用元件在SlLCY-B2启动子的分布 注:sgRNA: 绿色>示这些sgRNAs位于外显子绿色示sgRNA邻近PAM 12 nt 的种子序列在番茄全基因组上是唯一序列;黑色>示该sgRNA邻近PAM 12 nt 的种子序列在其它染色体的1个位点上有与其匹配的序列;灰色>表示这些sgRNAs横跨2个外显子邻接处或含有含连续的TTTT,选用pol III启动子尽力避免选用这些sgRNA序列。顺式作用元件:红色下划线示顺式作用元件位于正链,蓝色下划线示元件位于负链
Fig.4 The position of sgRNAs and cis-element in SlLCY-B2 promoter Note: sgRNA: Green shows these sgRNAs located in exon green seed sequence on the whole tomato genome; blue shows the seed sequence of the sgRNA adjacent PAM 12 nt has a matching sequence at one site of other chromosomes; grey indicates these sgRNAs across two exon neighbors or containing continuous TTTT, using pol III promoter to avoid these sgRNA sequences. Cis action element: red underscore element is located in the positive chain and blue underscore element in the negative chain
| [1] | 吕慧芳, 刘四运. 植物番茄红素生物合成及分子调控机理研究进展[J]. 池州学院学报, 2016, 30(3):43-47. |
| LV Huifang, LIU Siyun. Biosynthesis of lycopene from plants And advances in molecular regulation mechanism[J]. Journal of Chizhou University, 2016, 30(3):43-47. | |
| [2] |
Ronen G, Carmel-Goren L, Zamir D, et al. An alternative pathway to beta-carotene formation in plant chromoplasts discovered by map-based cloning of beta and old-gold color mutations in tomato[J], Proc. Natl. Acad. Sci., USA (PNAS). 2000, 97(20): 11102-11107.
DOI URL |
| [3] |
Rosati C, Aquilani R, Dharmapuri S et al. Metabolic engineering of beta-carotene and lycopene content in tomato fruit[J]. Plant J, 2000, 24:413-419.
DOI PMID |
| [4] | 马超, 马兵钢, 郝青南. 番茄红素β环化酶基因(Lyc-β)RNAi载体构建及表达鉴定[J]. 农业生物技术学报, 2010, 18(1): 10-17. |
| MA Chao, MA Binggang, HAO Qinnan. Construction of RNA Interference Vector for Lycopene Cyclase β Gene (Lyc-β) and its Expression Identification in Lycopersicun esculentum[J]. Journal of Agricultural Biotechnology, 2010, 18(1):10-17. | |
| [5] |
万群, 张兴国, 宋明. 果实特异性 RNAi 介导的 Lcy 基因沉默来增加番茄中番茄红素的含量[J]. 生物工程学报, 2007, 23(3): 429-433.
PMID |
|
WAN Qun, ZHANG Xinguo, SONG Min. Fruit-specific RNAi-mediated Lcy Gene Silencing Enhances Content of Lycopene in Tomatoes[J]. Chinese Journal of Biotechnology. 2007, 23(3): 429-433
DOI PMID |
|
| [6] |
Voytas D F. Plant genome engineering with sequence-specific nucleases[J]. Annu. Rev. Plant. Biol, 2013, 64(1):327-350.
DOI URL |
| [7] |
Li X, Wang Y, Chen S, et al. Lycopene is enriched in tomato fruit by CRISPR/Cas9-mediated multiplex genome editing[J]. Frontiers in Plant Science, 2018, 9:559.
DOI PMID |
| [8] |
Farboud B, Meyer B J. Dramatic enhancement of genome editing by CRISPR/Cas9 through improved guide RNA design[J]. Genetics, 2015, 199: 959-971.
DOI PMID |
| [9] |
Lescot M, Déhais P, Moreau Y, et al. PlantCARE: a database of plant cis-acting regulatory elements and a portal to tools for in silico analysis of promoter sequences[J]. Nucleic Acids Res, 2002, 30(1): 325-327.
DOI URL |
| [10] |
Arumuganathan K, Earle ED. Nuclear DNA content of some important plant species[J]. Plant Molecular Biology Reports, 1991, 9: 208-218.
DOI URL |
| [11] |
Fu Y, Foden J, Khayter C, et al. High-frequency off-target mutagenesis induced by CRISPR/Cas nucleases in human cells[J]. Nature Biotechnology, 2013, 31(9): 822-826.
DOI |
| [12] |
Hsu p, Scott D, Weinstein J, et al. DNA targeting specificity of RNA-guided Cas9 nucleases[J]. Nature Biotechnology, 2013, 31(9): 827-832.
DOI PMID |
| [13] |
Friedland, A. E., Y. B. Tzur, et al. Church et al. Heritable genome editing in C. elegans via a CRISPR-Cas9 system[J]. Nat. Methods, 2013, 10: 741-743.
DOI PMID |
| [14] |
Doudna J A, Charpentier E,. Genome editing. The new frontier of genome engineering with CRISPR-Cas9[J]. Science, 2014, 346 (6213): 1258096.
DOI URL |
| [15] |
Doench J G, Hartenian E, Graham D B, et al. Rational design of highly active sgRNAs for CRISPR/Cas9-mediated gene inactivation[J]. Natura Biotechnology, 2014, 32(12):1262-127.
DOI |
| [16] | Zhang S J, Zhang R Z, Song G Q, et al. Construction of promoter region CRISPR/Cas9 genome editing vector of pinb gene in wheat[J]. Shandong Agricultural Sciences, 2020, 52(1):1-9. |
| [17] | 张淑娟, 张荣志, 宋国琦, 等. 小麦 Pinb 基因启动子区 CRISPR / Cas9 基因编辑载体的构建[J]. 山东农业科学, 2020, 52(1):1-9. |
| ZHANG Sunjuan, ZHANG Rongzhi, SONG Guoqi, et al. Construction of promoter region CRISPR/Cas9 genome editing vector of pinb gene in wheat.Shandong Agricultural Sciences[J]. Shandong Agricultural Sciences, 2020, 52(1):1-9 | |
| [18] |
Rodríguez-Leal D, Lemmon Z H, Man J, et al. Engineering quantitative trait variation for crop improvement by genome editing[J]. Cell, 2017, 171(2): 470-480.
DOI PMID |
| [19] | Huang L, Li Q, Zhang C, et al. Creating novel Wx alleles with fine‐tuned amylose levels and improved grain quality in rice by promoter editing using CRISPR/Cas9 system[J]. Plant Biotechnology Journal, 2020a, https://doi.org/10.1111/pbi.13391. |
| [20] | Huang L, Sreenivasulu N, Liu Q. Waxy editing: Old meets new[J]. Trends in Plant Science,2020b https://doi.org/10.1016/j.tplants.2020.07.009. |
| [1] | 王丹丹, 李燕, 张庆银, 李世东, 庞永超, 马琨芝, 马龙, 牛瑞生, 钟增明, 齐连芬, 师建华. 不同微生物菌处理对番茄土壤微生物多样性的影响[J]. 新疆农业科学, 2023, 60(9): 2248-2257. |
| [2] | 蒲敏, 阮向阳, 肖乐乐, 索常凯, 陈国永, 冶军, 高波. 枸溶性钙镁肥对加工番茄钙、镁吸收及品质的影响[J]. 新疆农业科学, 2023, 60(8): 1987-1995. |
| [3] | 肖林刚, 马艳, 宋兵伟, 焦锐斌, 邢剑飞. 温室膜下微喷灌溉技术研究进展[J]. 新疆农业科学, 2023, 60(7): 1731-1740. |
| [4] | 杜红艳, 庞胜群, 马海翔, 吉雪花. 加工番茄早熟突变体农艺性状相关性及通径分析[J]. 新疆农业科学, 2023, 60(4): 943-950. |
| [5] | 朱普生, 刘慧英, 曹泽, 刘凯歌, 李雪珍. 外源GSNO对NaCl胁迫下番茄幼苗生长及光合特性的影响[J]. 新疆农业科学, 2023, 60(2): 351-358. |
| [6] | 曾军, 武磊, 高雁, 张卓, 林青, 刘建伟, 杨红梅, 霍向东, 史应武. 光合细菌叶面肥喷施对设施有机番茄产量和品质的影响[J]. 新疆农业科学, 2023, 60(12): 3018-3024. |
| [7] | 刘升学, 李思琪, 王晓东, 杨德松. 番茄早疫病菌dsRNA多样性分析[J]. 新疆农业科学, 2023, 60(12): 3057-3064. |
| [8] | 芦大伟, 哈丽哈什·依巴提, 李青军. 磷肥用量对滴灌加工番茄产量、品质及磷肥利用率的影响[J]. 新疆农业科学, 2023, 60(1): 185-191. |
| [9] | 李岳雁, 李玉姗, 王帆, 郭雅文, 王飞燕, 高杰, 宋羽. 不同品种番茄果实性状遗传多样性及聚类分析[J]. 新疆农业科学, 2022, 59(9): 2147-2157. |
| [10] | 李春雨, 谭占明, 程云霞, 束胜, 何涛, 靳钰婕, 马新超, 杜佳庚, 张婧. 水肥耦合对沙培番茄生长发育及品质的影响[J]. 新疆农业科学, 2022, 59(9): 2158-2169. |
| [11] | 马雪红, 刘婷, 李传天, 朱金芳. HPLC法测定番茄红素胶束中番茄红素Z/E异构体含量[J]. 新疆农业科学, 2022, 59(9): 2209-2216. |
| [12] | 古宁宁, 张蒲, 谢彦如, 唐丹, 赵志信, 董瑞芳, 崔拥民, 秦勇. 基质中化肥施入量对番茄幼苗生长的影响[J]. 新疆农业科学, 2022, 59(8): 1929-1934. |
| [13] | 许俊锋, 杨蓉, 詹发强, 侯敏, 包慧芳, 王宁, 龙宣杞, 张志东, 崔卫东. 有机-无机液体复合肥功能菌筛选及对设施番茄品质、生理活性的影响[J]. 新疆农业科学, 2022, 59(7): 1758-1766. |
| [14] | 王强, 刘会芳, 韩宏伟, 庄红梅, 王柏柯, 王娟, 杨涛, 王浩, 秦勇. 基于 TMT和PRM 技术筛选番茄响应盐胁迫差异表达蛋白[J]. 新疆农业科学, 2022, 59(6): 1418-1428. |
| [15] | 林青, 史应武, 王娜, 华兰兰, 杨红梅, 楚敏, 曾军, 高雁, 霍向东. 加工番茄系统抗性诱导促生菌的筛选鉴定及其促生防病效果[J]. 新疆农业科学, 2022, 59(6): 1466-1474. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||