

新疆农业科学 ›› 2022, Vol. 59 ›› Issue (6): 1321-1329.DOI: 10.6048/j.issn.1001-4330.2022.06.003
杨静1( ), 王为然1, 王萌1, 朱家辉1, 宁新民1, 阿里甫·艾尔西1, 闵玲2(
), 王为然1, 王萌1, 朱家辉1, 宁新民1, 阿里甫·艾尔西1, 闵玲2( ), 孔杰1,3(
), 孔杰1,3( )
)
收稿日期:2021-10-11
出版日期:2022-06-20
发布日期:2022-07-07
通信作者:
闵玲,孔杰
作者简介:杨静(1989-),女,陕西宁强人,助理研究员,研究方向为长绒棉遗传育种. (E-mail) hzjingy@126.com
基金资助:
YANG Jing1( ), WANG Weiran1, WANG Meng1, ZHU Jiahui1, NING Xinmin1, Alifu Aierxi1, MIN Ling2(
), WANG Weiran1, WANG Meng1, ZHU Jiahui1, NING Xinmin1, Alifu Aierxi1, MIN Ling2( ), KONG Jie1,3(
), KONG Jie1,3( )
)
Received:2021-10-11
Online:2022-06-20
Published:2022-07-07
Correspondence author:
MIN Ling, KONG Jie
Supported by:摘要:
【目的】 研究新疆海岛棉不同材料愈伤组织培养体系,筛选再生能力强的海岛棉材料,为新疆海岛棉基因工程育种提供参考。【方法】 以105份新疆海岛棉为材料,利用改良后的MS培养基对下胚轴共培养,在2,4-D诱导培养基中诱导分化产生愈伤组织,浸染农杆菌介导的红色荧光蛋白,验证转化效果。【结果】 海岛棉材料愈伤组织的增殖速率与其基因型有关,改良后的MS共培养基、2,4-D诱导培养基可有效用于新疆海岛棉共培养和胚性愈伤组织增殖;愈伤组织增殖的适宜培养时间为4个月,时间过长不利于其增殖;愈伤增殖速度与转化率呈正相关,增殖快的材料其红色荧光蛋白的转化率较高;筛选出2份增殖快且转化率好的海岛棉材料。【结论】 建立了新疆海岛棉胚性愈伤组织培养体系与鉴定方法,筛选出9份愈伤增殖好、且能够有效转化的海岛棉材料。
中图分类号:
杨静, 王为然, 王萌, 朱家辉, 宁新民, 阿里甫·艾尔西, 闵玲, 孔杰. 新疆海岛棉胚性愈伤组织培养体系[J]. 新疆农业科学, 2022, 59(6): 1321-1329.
YANG Jing, WANG Weiran, WANG Meng, ZHU Jiahui, NING Xinmin, Alifu Aierxi, MIN Ling, KONG Jie. Preliminary Study on the Embryogenic Callus Culture System of Xinjiang Island Cotton (G. barbadense L. )[J]. Xinjiang Agricultural Sciences, 2022, 59(6): 1321-1329.
| 材料编号Material code | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 907 | 947 | 966 | 974 | 984 | 1011 | 1028 | 1046 | 1061 | 1074 | 1086 | 1094 | 1108 | 1119 |
| 920 | 954 | 967 | 975 | 987 | 1012 | 1036 | 1050 | 1062 | 1075 | 1087 | 1098 | 1109 | |
| 921 | 955 | 968 | 976 | 995 | 1013 | 1040 | 1051 | 1063 | 1076 | 1088 | 1099 | 1111 | |
| 922 | 960 | 969 | 977 | 998 | 1014 | 1041 | 1052 | 1064 | 1080 | 1089 | 1101 | 1112 | |
| 923 | 961 | 970 | 979 | 999 | 1016 | 1042 | 1056 | 1065 | 1081 | 1090 | 1102 | 1113 | |
| 926 | 962 | 971 | 980 | 1007 | 1017 | 1043 | 1058 | 1067 | 1083 | 1091 | 1103 | 1115 | |
| 927 | 964 | 972 | 981 | 1008 | 1024 | 1044 | 1059 | 1070 | 1084 | 1092 | 1104 | 1116 | |
| 933 | 965 | 973 | 982 | 1010 | 1025 | 1045 | 1060 | 1073 | 1085 | 1093 | 1105 | 1118 | |
表1 海岛棉试验材料
Table 1 The experiment accessions of island cotton
| 材料编号Material code | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 907 | 947 | 966 | 974 | 984 | 1011 | 1028 | 1046 | 1061 | 1074 | 1086 | 1094 | 1108 | 1119 |
| 920 | 954 | 967 | 975 | 987 | 1012 | 1036 | 1050 | 1062 | 1075 | 1087 | 1098 | 1109 | |
| 921 | 955 | 968 | 976 | 995 | 1013 | 1040 | 1051 | 1063 | 1076 | 1088 | 1099 | 1111 | |
| 922 | 960 | 969 | 977 | 998 | 1014 | 1041 | 1052 | 1064 | 1080 | 1089 | 1101 | 1112 | |
| 923 | 961 | 970 | 979 | 999 | 1016 | 1042 | 1056 | 1065 | 1081 | 1090 | 1102 | 1113 | |
| 926 | 962 | 971 | 980 | 1007 | 1017 | 1043 | 1058 | 1067 | 1083 | 1091 | 1103 | 1115 | |
| 927 | 964 | 972 | 981 | 1008 | 1024 | 1044 | 1059 | 1070 | 1084 | 1092 | 1104 | 1116 | |
| 933 | 965 | 973 | 982 | 1010 | 1025 | 1045 | 1060 | 1073 | 1085 | 1093 | 1105 | 1118 | |

图1 海岛棉愈伤组织诱导转化过程 注:A.陆地棉Jin668无菌苗(CK);B.Jin668下胚轴;C.海岛棉无菌苗;D~F.923、971、962下胚轴。Bars 值均为1 cm
Fig.1 Process of callus induction and transformin island cotton Note: A.The aseptic seedling of Jin668; B.Jin668 hypocotyl; C.The aseptic seedling of island cotton; D-F.Hypocotyl of 923,971,962.Bars value is 1 cm
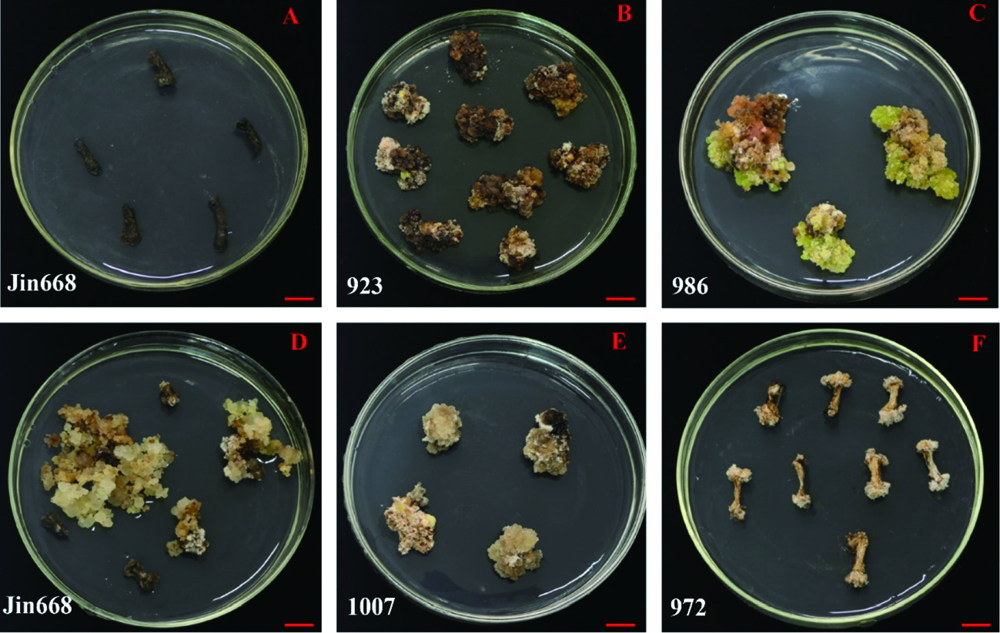
图2 愈伤组织增殖 注:A.未浸染农杆菌的陆地棉Jin668(CK)的愈伤组织;B~C,E~F.培养4个月后的愈伤组织;D.Jin668浸染农杆菌后培养4个月的愈伤组织。Bars值均为1 cm
Fig.2 Callus induction and proliferation Note: A.Callus of upland cotton Jin668 (CK) not infested with agrobacterium; B-C,E-F, Callus of 923,986,1007 and 972 after 4 months of culture,respectively.D.The callus of Jin668 after 4 months of cultivation inoculation with agrobacterium.Bars value is 1 cm
| 材料编号 Code | 诱导4个月增重 Add weight after 4 months(g) | 愈伤颜色质地 Callus of color and phenotype | 愈伤细胞形态 Callus of cell morphology | 诱导6个月增重 Add weight after 6 months(g) | 愈伤颜色质地 Callus of color and phenotype | 愈伤细胞形态 Callus of cell morphology |
|---|---|---|---|---|---|---|
| Jin668 | 0.26±0.08 | 浅黄,疏松 | 长柱、近球形 | 0.35±0.04 | 浅棕,疏松 | 长柱形 |
| 962 | 0.13±0.02 | 浅黄色,疏松 | 同上 | 0.64±0.15 | 浅黄,疏松 | 近球、长柱形 |
| 1010 | 0.22±0.04 | 粉白色,硬 | 同上 | 0.83±0.15 | 浅绿,硬 | 同上 |
| 1025 | 0.35±0.06 | 浅绿色,疏松 | 同上 | 0.47±0.10 | 浅绿色,疏松 | 同上 |
| 1052 | 0.24±0.07 | 浅绿色,硬 | 同上 | 0.35±0.13 | 红褐色,疏松 | 同上 |
| 964 | 0.20±0.06 | 绿色,疏松 | 近球形 | 1.10±0.14 | 浅黄,软 | 近球形 |
| 986 | 0.12±0.03 | 绿色,硬 | 同上 | 0.45±0.10 | 浅黄,疏松 | 同上 |
| 1011 | 0.16±0.06 | 浅绿,硬 | 同上 | 0.29±0.04 | 浅黄,硬 | 同上 |
| 1086 | 0.10±0.01 | 浅绿,疏松 | 同上 | 0.18±0.03 | 浅绿,硬 | 同上 |
| 1103 | 0.18±0.03 | 同上 | 同上 | 0.39±0.05 | 浅绿,硬 | 同上 |
表2 不同诱导时间下胚轴愈伤组织质量(部分)
Table 2 Callus quality of hypocotyl at different induction time
| 材料编号 Code | 诱导4个月增重 Add weight after 4 months(g) | 愈伤颜色质地 Callus of color and phenotype | 愈伤细胞形态 Callus of cell morphology | 诱导6个月增重 Add weight after 6 months(g) | 愈伤颜色质地 Callus of color and phenotype | 愈伤细胞形态 Callus of cell morphology |
|---|---|---|---|---|---|---|
| Jin668 | 0.26±0.08 | 浅黄,疏松 | 长柱、近球形 | 0.35±0.04 | 浅棕,疏松 | 长柱形 |
| 962 | 0.13±0.02 | 浅黄色,疏松 | 同上 | 0.64±0.15 | 浅黄,疏松 | 近球、长柱形 |
| 1010 | 0.22±0.04 | 粉白色,硬 | 同上 | 0.83±0.15 | 浅绿,硬 | 同上 |
| 1025 | 0.35±0.06 | 浅绿色,疏松 | 同上 | 0.47±0.10 | 浅绿色,疏松 | 同上 |
| 1052 | 0.24±0.07 | 浅绿色,硬 | 同上 | 0.35±0.13 | 红褐色,疏松 | 同上 |
| 964 | 0.20±0.06 | 绿色,疏松 | 近球形 | 1.10±0.14 | 浅黄,软 | 近球形 |
| 986 | 0.12±0.03 | 绿色,硬 | 同上 | 0.45±0.10 | 浅黄,疏松 | 同上 |
| 1011 | 0.16±0.06 | 浅绿,硬 | 同上 | 0.29±0.04 | 浅黄,硬 | 同上 |
| 1086 | 0.10±0.01 | 浅绿,疏松 | 同上 | 0.18±0.03 | 浅绿,硬 | 同上 |
| 1103 | 0.18±0.03 | 同上 | 同上 | 0.39±0.05 | 浅绿,硬 | 同上 |

图4 愈伤组织增殖较好的海岛棉 注:A~H分别为962,964,1010,1011,1025,1052,1086和1103培养4个月后的愈伤组织。Bars值均为1 cm
Fig.4 The better callus induction and proliferation of accessions Note:A.The callus of 962,964,1010,1011,1025,1052,1086 and 1103 after 4 months of cultivation,respectively.Bars value is 1 cm
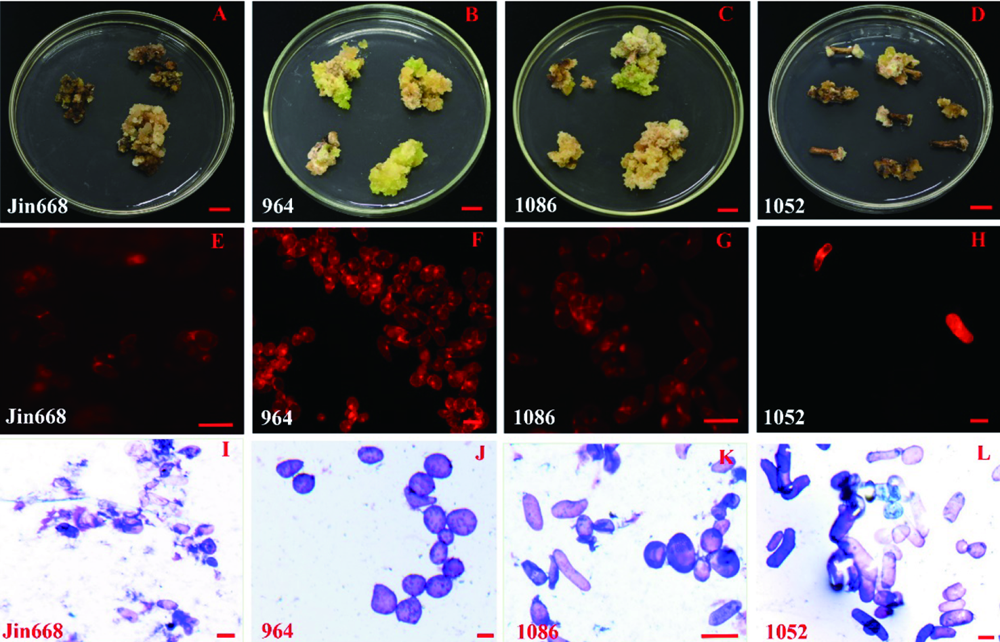
图5 海岛棉红色荧光蛋白转化 注:A~D.Jin668、964、1086和1052培育4个月后的愈伤组织;E~H.Jin668、964、1086和1052培育4个月愈伤组织中的红色荧光蛋白;I~L.Jin668、964、1086和1052培育4个月后愈伤组织的细胞形态(甲苯胺蓝染色).A,B,C,D的bars值为1cm,E、F、G、H、I、J、K、L为100 μm
Fig.5 Observation of red fluorescence protein transform in island cotton Note:A-D.Callus of Jin668,964,1086 and 1052 cultivated 4 Callus after 4 months, respectively; E-H.Jin668,964,1086 and 1052 after 4 months of cultivation of red fluorescent protein in callus; I-L.Jin668, 964,1086 and 1052 after 4 months of cultivation tissue cell morphology (toluidine blue staining), respectively.Bars value of A, B, C, D is 1 cm, and E, F, G, H,I,J,K, L is 100 μm

图6 红色荧光蛋白转化率较低的下胚轴增殖变化 注:A,D.海岛棉1010和1103培育4个月后的愈伤组织;B,E.1010和1103培育4个月后愈伤组织中的红色荧光蛋白;C,F:1010和1103培育4个月后愈伤组织的细胞形态(甲苯胺蓝染色).A和D的bars值为1 cm,B、C、E、F为100 μm
Fig.6 Observation of lower transform ratio of red fluorescence protein in island cotton Note:A, D: Island cotton 1010and 1103 callus after 4 months of cultivation; B, E: 1010 and1103 callus after 4 months of cultivation of red fluorescence protein; C, F: 1010 and 1103 callus cell morphology after 4 months of cultivation (toluidine blue staining).Bars value of A and D is 1cm, B, C, E, and F is 100 μm
| [1] | Huang X, OUYANG X, DENG X W. Beyond repressionof photomorphogenesis: role switching of COP/DET/FUS in light signaling[J]. Current Opinion Plant Biology, 2014, 21C: 96-103. |
| [2] | Beasley C A. In vitro culture of fertilized cotton ovules[J]. Bio Science, 1971, 21(17):906-907. |
| [3] |
Davidonis G H, Hamilton R H. Plant regeneration from callus tissue of Gossypium hirsutum L.[J]. Plant Science Letters, 1983, 32:89-93.
DOI URL |
| [4] |
Keller G, Spatola L, McCabe D E, et al.(1997). Transgenic cotton resistant to herbicide bialaphos[J]. Transgenic Research, 6:385-392.
DOI URL |
| [5] | 武秀明, 刘传亮, 张朝军, 等. 棉花体细胞胚胎发生的研究进展[J]. 植物学通报, 2008, 25(4):469-475. |
| WU Xiuming, LIU Chuanliang, ZHANG Chaojun, et al. Progress of Somatic Embryogenesis in Cotton[J]. Chinese Bulletin of Botany, 2008, 25(4):469-475. | |
| [6] | 谭晓连, 钱迎倩. 不同外植体来源和培养条件对拟似棉植株再生的影响[J]. 遗传学报, 1988, 15(2): 81-85. |
| TAN Xiaolian, QIAN Yingqian. Effects of explant sources and culture conditions on plant regeneration in (G.gossypioides Ulbrich) Standley[J]. Journal of Genetics and Genomics, 1998, 15(2): 81-85. | |
| [7] |
Sun Y, Zhang X, Jin S, et al. Somatic embryogenesis and plant regeneration in wild cotton (Gossypiumklotzschianum)[J]. Plant Cell, Tissue and Organ Culture, 2003, 75(3): 247-253.
DOI URL |
| [8] | 陆振鑫, 夏镇澳. 戴维逊棉的组织培养与原生质体培养研究[J]. 植物学报, 1991, 33(2):98-103, 172. |
| LU Zhenxin, XIA Zhenao. Study on tissue and protoplast culture of wild cotton (Gossypium davidsonil)[J]. Chinese Bulletin of Botany, 1991, 33(2):98-103, 172. | |
| [9] |
Sun Y, Zhang X, Huang C, et al. Somatic embryogenesis and plant regeneration from different wild diploid cotton (Gossypium) species[J]. Plant Cell Reports, 2006, 25(4): 289-296.
DOI URL |
| [10] | Rao A Q, Hussain S S, Shahzad M S, et al. Somatic embryogenesis in wild relatives of cotton (Gossypium spp.)[J]. Journal of Zhejiang University Science Botany, 2006, 7(4):291-298. |
| [11] |
Yan S, Zhang Q, Wang J, et al. Somatic embryogenesis and plant regeneration in two wild cotton species belong to G genome[J]. In Vitro Cellular and Developmental Biology-Plant, 2010, 46(3): 298-305.
DOI URL |
| [12] | 魏延红. 农杆菌介导海岛棉(G.barbadense L.)遗传转化技术研究[D]. 石河子: 石河子大学, 2013. |
| WEI Yanhong. Agrobacterium-mediated Sea-island cotton (G.barbadense L.) Genetic transformation technology research[D]. Shihezi: Shihezi University 2013. | |
| [13] | 周小凤, 金双侠, 李翔, 等. 新疆海岛棉的丛生芽诱导和茎尖遗传转化的研究[J]. 棉花学报, 2009, 21(4):324-329. |
| ZHOU Xiaofeng, JIN Shuangxia, LI Xiang, et al. Multiple-shoot Induction and Genetic Transformation of Island Cotton (G.barbadense L.) in Xinjiang[J]. Cotton Science, 2009, 21(4):324-329. | |
| [14] | 丁喜莲. 农杆菌介导的海岛棉转Bt基因遗传转化研究[D]. 乌鲁木齐: 新疆农业大学, 2015. |
| DING Xilian. Study on the Agrobacterium tumefaciens-mediated Transformation of Bt Gene into Sea Island Cotton (G.barbadense L.)[D]. Urumqi: Xinjiang Agricultural University, 2015. | |
| [15] |
Navarro C, E Cruz-Oró, Prat S. Conserved function of FLOWERING LOCUS T (FT) homologues as signals for storage organ differentiation[J]. Current Opinion in Plant Biology, 2015, 23:45-53.
DOI URL |
| [16] |
Jin S X, Zhang X L, Nie Y C, et al. Identification of a novel elite genotype for in vitro culture and genetic transformation of cotton.[J]. Biologia Plantarum, 2006, 50(4):519-524.
DOI URL |
| [17] | Cristina Navarro, Eduard CruzOró, SaloméPratNavarro C. Conserved function of FLOWERING LOCUST(FT) homologues as signals for storage organ differentiation.[J]. Current Opinion Plant Biology, 2014, 23C:45-53. |
| [18] | 郑顺利, 陈金湘, 周仲华. 影响棉花愈伤组织及其体细胞胚发生的内外因素[J]. 棉花科学, 2012, 34(1),1-10. |
| ZHENG Shunli, CHEN Jinxiang, ZHOU Zhonghua. Internal and External Factors of Cotton Callus and Its Somatic Embryogenesis[J]. Cotton Science, 2012, 34(1):1-10. | |
| [19] | 商海红, 刘传亮, 张朝军, 等. 棉花体细胞胚发生机理的研究进展[J]. 西北植物学报, 2009, 29(3):637-642. |
| SHANG Haihong, LIU Chuanliang, ZHANG Chaojun, et al. Progress in Mechanisms of Cotton Somatic Embryogenesis[J]. Acta Botanica Boreali-Occidentalia Sinica, 2009, 29(3):637-642. | |
| [20] | 师海荣, 王清连, 鲁玉贞. 陆地棉品种在体细胞培养中愈伤组织褐化的生化基础研究[J]. 中国农学通报, 2006, 22(6):215-217. |
| SHI Hairong, WANG Qinglian, LU Yuzhen. Study on Physiological biochemistry of Callus Browning in Three Upland Cottons[J]. Chinese Agricultural Science Bulletin, 2006, 22(6):215-217. | |
| [21] | 张朝军, 李付广, 王玉芬, 等. 降低棉花胚性愈伤褐化研究[J]. 棉花学报, 2005, 17 (5):285-288. |
| ZHANG Chaojun, LI Fuguang, WANG Yufen, et al. Prevent Browning of Upland Cotton Embryoid Callus[J]. Cotton Science, 2005, 17(5):285-288. | |
| [22] | 杨瑞思, 周静, 张霞. 海岛棉(Gossypium barbadense)体细胞胚发生体系中的畸形再生植株的遗传性分析[J]. 分子植物育种, 2019, 17,(23)7849-7853. |
| YANG Ruisi, ZHOU Jing, ZHANG Xia. Genetic analysis of malformed regenerated seedlings in the somaticembryogenesisof Gossypium barbadense[J]. Molecular Plant Breeding, 2019, 17(23):7849-7853. | |
| [23] | 翁琴, 陈全家, 孔庆平, 等. 农杆菌介导的海岛棉茎尖再生体系及其遗传转化影响因子的研究[J], 新疆农业大学学报, 2007, 30(4) :63-67. |
| WENG Qin, CHEN Quanjia, KONG Qingping, et al. Study on Regeneration System and Influencing Factorsof Genetic Transformation of G.barbadense Shoot Apex Mediated by Agrobacterium[J]. Journal of Xinjiang Agricultural University, 2007, 30(4): 63-67. |
| [1] | 段松江, 彭增莹, 申莹莹, 木丽迪尔·拜波拉提, 吴一凡, 崔建平, 张巨松. 不同海岛棉品种产量及纤维品质对氮肥的响应[J]. 新疆农业科学, 2023, 60(7): 1569-1579. |
| [2] | 付强, 王琴, 徐彩芹, 牛俊丽, 牛建新, 王建友. 黑核桃组培中消毒及防止褐化最适浓度分析[J]. 新疆农业科学, 2023, 60(6): 1499-1505. |
| [3] | 秦国礼, 王为然, 王萌, 杨静, 黄幸磊, 刘志清, 朱家辉, 阿里甫·艾尔西, 孔杰, 陈国栋. 草甘膦对海岛棉农艺性状及光合作用的影响[J]. 新疆农业科学, 2023, 60(12): 2861-2868. |
| [4] | 刘晨曦, 朱雨婷, 周强, 陈瑾, 赵文杰, 郑凯. 海岛棉β-胡萝卜素异构酶GbD27-6基因克隆及表达分析[J]. 新疆农业科学, 2023, 60(12): 2869-2877. |
| [5] | 宋吉坤, 辛玥, 李龙云, 刘国元, 裴文锋, 马建江, 曲延英, 于霁雯, 吴嫚. 利用基因芯片分析比较Giza75和SG747纤维发育差异表达基因[J]. 新疆农业科学, 2022, 59(6): 1312-1330. |
| [6] | 杨龙, 赵福相, 段雅洁, 蔡永生, 郑凯, 陈琴, 陈全家, 曲延英. 海岛棉重组自交系群体花铃期抗旱性评价[J]. 新疆农业科学, 2022, 59(12): 2861-2869. |
| [7] | 陆小双, 张梦洁, 韩万里, 龙遗磊, 刘鹏飞, 陈全家, 曲延英, 邓晓娟. 海岛棉抗枯萎病性状与 SSR标记的关联分析[J]. 新疆农业科学, 2022, 59(10): 2365-2373. |
| [8] | 闵凯丽, 晁祥保, 滕露, 蔡永生, 雷慧辰, 严中建, 郑凯, 陈全家. 海岛棉GbHCT10基因的克隆与表达分析[J]. 新疆农业科学, 2021, 58(2): 206-215. |
| [9] | 苏秀娟, 徐海江, 邓晓娟, 龚林涛. 盐胁迫对海岛棉种子活力的影响[J]. 新疆农业科学, 2020, 57(9): 1604-1614. |
| [10] | 王天友, 冯春晖, 王有武, 曹新川, 郭伟锋, 刘春艳, 黄光伟, 何良荣. 海岛棉不同果枝类型杂交F2代产量品质性状分布规律[J]. 新疆农业科学, 2020, 57(2): 209-218. |
| [11] | 张炎, 姚银坤, 胡伟, 高媛, 汤明尧. 施磷对棉花磷素积累、分配、利用及产量的影响[J]. 新疆农业科学, 2020, 57(11): 2004-2011. |
| [12] | 赵福相, 刘康永, 曲延英, 高文伟, 陈全家. 海岛棉种质资源抗旱性评价[J]. 新疆农业科学, 2019, 56(7): 1188-1196. |
| [13] | 陈振, 张巨松, 严青青, 杨培, 张玮涛. 不同基因型海岛棉根系形态参数对混合盐碱胁迫的响应[J]. 新疆农业科学, 2019, 56(11): 1961-1970. |
| [14] | 王为然, 杨静, 朱家辉, 张延辉, 宁新民, 刘志清, 孔杰, 阿里甫·艾尔西. 新疆零式果枝海岛棉掉絮原因分析[J]. 新疆农业科学, 2019, 56(11): 1979-1987. |
| [15] | 孔杰, 王为然, 张延辉, 朱家辉, 杨静, 宁新民, 阿里甫·艾尔西, 华金平. 海岛棉熟性及其高关联农艺性状与生态因子的关系[J]. 新疆农业科学, 2018, 55(5): 785-796. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||